2025年10月28日���,上海交通大學(xué)章雪晴團(tuán)隊(duì)與新澤西理工學(xué)院許曉陽(yáng)團(tuán)隊(duì)在期刊《ACS Nano》上發(fā)表題為" mRNA-Based Vaccination Drives in Vivo Dendritic Cell Reprogramming and Selective Cytotoxic T Lymphocyte Modulation for Enhanced Antitumor Immunity "的研究論文。

借助艾特森MPE-L2型微流控制備儀��,研究團(tuán)隊(duì)成功開(kāi)發(fā)了一種“疫苗啟動(dòng)選擇性T細(xì)胞調(diào)控(VISIT)”平臺(tái)�。首先通過(guò)艾特森微流控制備儀制備mRNA-LNP脂質(zhì)納米顆粒,將編碼腫瘤抗原以及膜結(jié)合型IL?15/IL?15Rα復(fù)合物(bIL?15�����,為IL?15的生物活性形式)的mRNA選擇性遞送至脾臟DC�����。系統(tǒng)給藥后�,VISIT平臺(tái)成功實(shí)現(xiàn)DC的體內(nèi)重編程�����,使其同步在細(xì)胞表面呈現(xiàn)抗原/MHC?I復(fù)合物與bIL?15。

研究背景
抗原特異性細(xì)胞毒性T淋巴細(xì)胞(CTLs)是抗腫瘤免疫的核心��,但高效抗原呈遞策略缺乏�、抗原特異性CD8+T細(xì)胞活化與擴(kuò)增不足,制約了腫瘤免疫治療發(fā)展���。傳統(tǒng)的樹(shù)突狀細(xì)胞(DC)體外疫苗和過(guò)繼性T細(xì)胞療法存在產(chǎn)量低、半衰期短�����、制備復(fù)雜且成本高的缺陷�����;而IL-15雖能促進(jìn)T細(xì)胞存活增殖�����,但其全身給藥會(huì)引發(fā)非特異性免疫激活,存在脫靶副作用。因此����,亟需開(kāi)發(fā)可在體內(nèi)靶向重編程DC�、同步呈遞腫瘤抗原與IL-15的策略����,以精準(zhǔn)激活抗原特異性CTLs。
1.疫苗介導(dǎo)的選擇性T細(xì)胞調(diào)控(VISIT)平臺(tái)
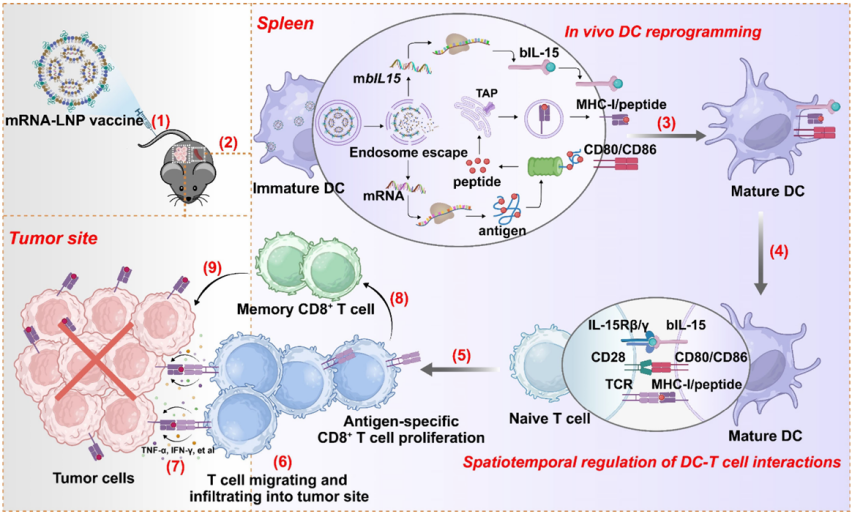
圖例1:疫苗介導(dǎo)的選擇性T細(xì)胞調(diào)控(VISIT)平臺(tái)
? mRNA-LNP制備過(guò)程:
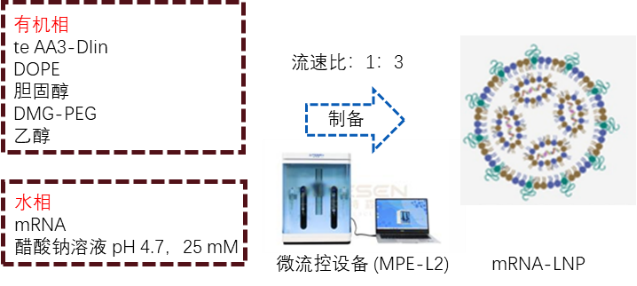
圖例2:mRNA-LNP制備過(guò)程
2. mRNA-LNP疫苗的設(shè)計(jì)與表征
研究團(tuán)隊(duì)成功合成可生物降解的脂質(zhì)te-AA3-Dlin,以此為基礎(chǔ)通過(guò)微流控技術(shù)制備mRNA-LNP����,平均粒徑~110nm����、表面電位近中性(-4 mV)�、mRNA包封率90%�����,血清中24h穩(wěn)定且抗RNase A降解�,對(duì)BMDC無(wú)毒性���。
該mRNA-LNP經(jīng)靜脈注射后>96%熒光信號(hào)富集于脾臟��,主要轉(zhuǎn)染脾臟 DC(~33% DC表達(dá)EGFP)����,究其原因在于te- AA3-Dlin LNP表面吸附的結(jié)構(gòu)蛋白-1(talin-1)DC 整合素受體,且ApoE占比低以避肝靶向。

圖例3:mRNA-LNP疫苗的設(shè)計(jì)與表征
3. 疫苗體內(nèi)誘導(dǎo)抗原特異性免疫應(yīng)答的驗(yàn)證
對(duì)C57BL/6J小鼠進(jìn)行三次免疫后��,mOVA-LNP和mOVA/bIL15-LNP 組脾臟中 SIINFEKL-H-2Kb+DC占比顯著升高(為PBS組的2.8-3.0 倍)����,且 mOVA/bIL15-LNP組可誘導(dǎo)更高比例的抗原特異性CD8+T 細(xì)胞(tetramer+CD8+T細(xì)胞占比為 mOVA-LNP 組的2倍),同時(shí)促進(jìn)效應(yīng)記憶性CD8+T細(xì)胞(TEM)分化、提升OVA特異性IgG抗體滴度���。

圖例4:mOVA/bIL15-LNP體內(nèi)促進(jìn)DC活化、抗原呈遞及抗原特異性免疫應(yīng)答
4. 疫苗體內(nèi)抗腫瘤療效驗(yàn)證-預(yù)防性模型
在MC38-OVA結(jié)腸癌模型中,mOVA/bIL15-LNP免疫可實(shí)現(xiàn)腫瘤緩解,且100天后再次挑戰(zhàn)腫瘤���,所有免疫小鼠仍無(wú)復(fù)發(fā),表明強(qiáng)大的記憶性T細(xì)胞儲(chǔ)備已建立。對(duì)非OVA表達(dá)的MC38腫瘤也有一定抑制效果(25%無(wú)瘤)��,證實(shí)其可誘導(dǎo)長(zhǎng)效抗原特異性免疫記憶����。
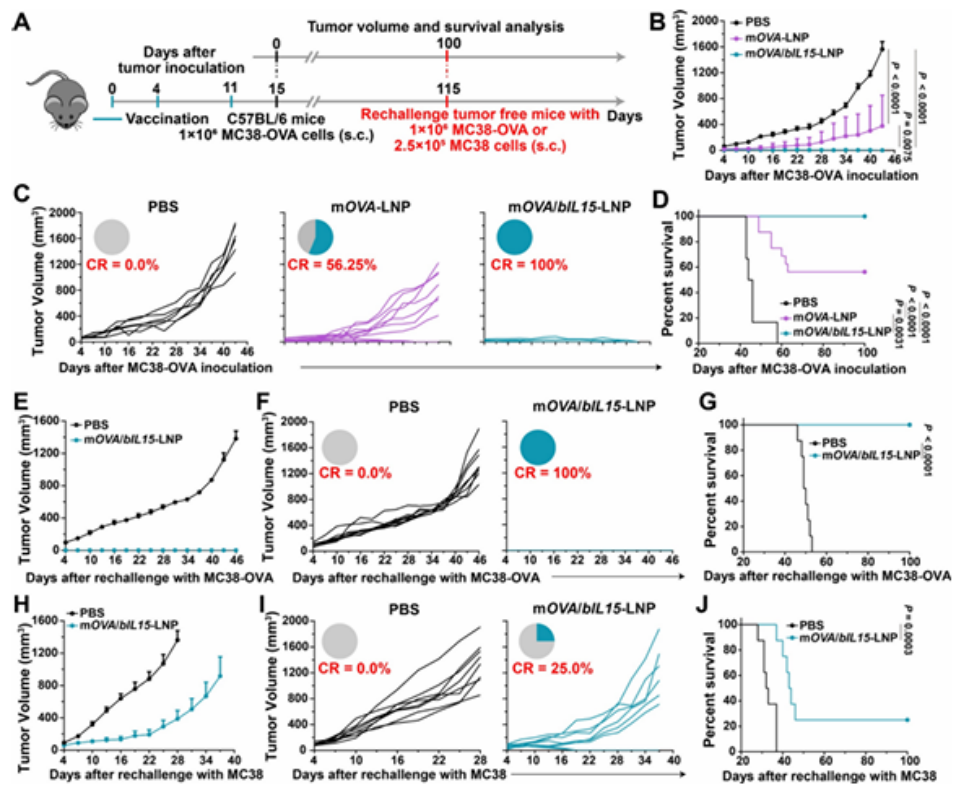
圖例5:mOVA/bIL15-LNP 預(yù)防性免疫及腫瘤再攻擊保護(hù)效果
5.疫苗體內(nèi)抗腫瘤療效驗(yàn)證-治療性模型
在已建立的MC38-OVA腫瘤模型中,靜脈注射mOVA/bIL15-LNP的抑瘤效果優(yōu)于肌內(nèi)注射�����,可使腫瘤重量降低89.6%��,并顯著延長(zhǎng)小鼠中位生存期;在B16F10黑色素瘤模型中�����,靶向TRP2抗原的 mTRP2/bIL15-LNP可顯著提升腫瘤組織中CD8+T細(xì)胞浸潤(rùn)�����、降低 Treg比例���,同時(shí)上調(diào)IL-6����、TNF-α���、IFN-γ等促炎因子水平�,延緩腫瘤進(jìn)展并延長(zhǎng)生存期。
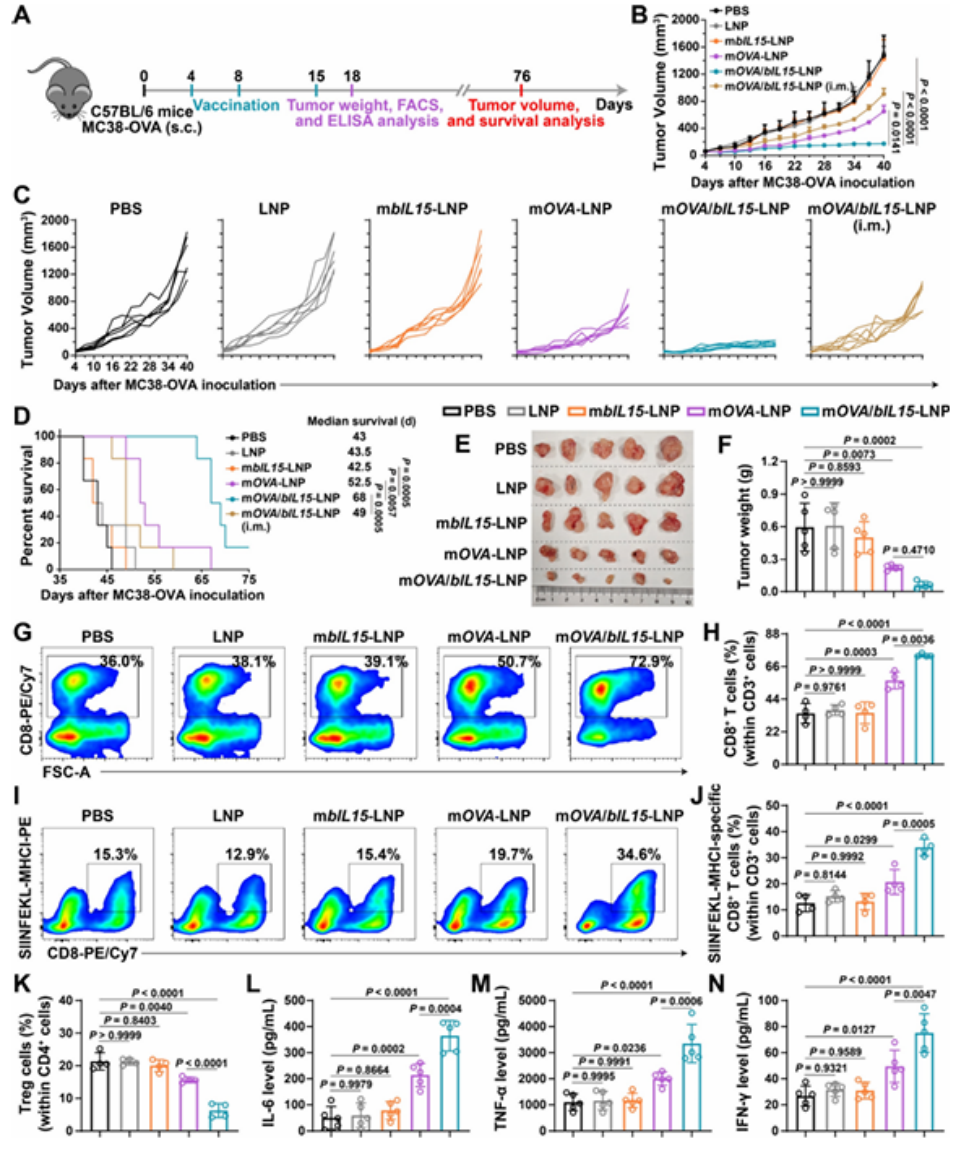
圖例6:mOVA/bIL15-LNP在已建立MC38-OVA腫瘤模型中的治療效果

圖例7:mTRP2/bIL15-LNP在B16F10黑色素瘤模型中的治療效果
6. 疫苗體內(nèi)抗腫瘤療效驗(yàn)證-聯(lián)合治療
mTRP2/bIL15-LNP與抗PD-1抗體聯(lián)用��,可協(xié)同增強(qiáng)B16F10模型的抑瘤效果���,腫瘤體積較單藥組顯著降低�,小鼠中位生存期進(jìn)一步延長(zhǎng)。
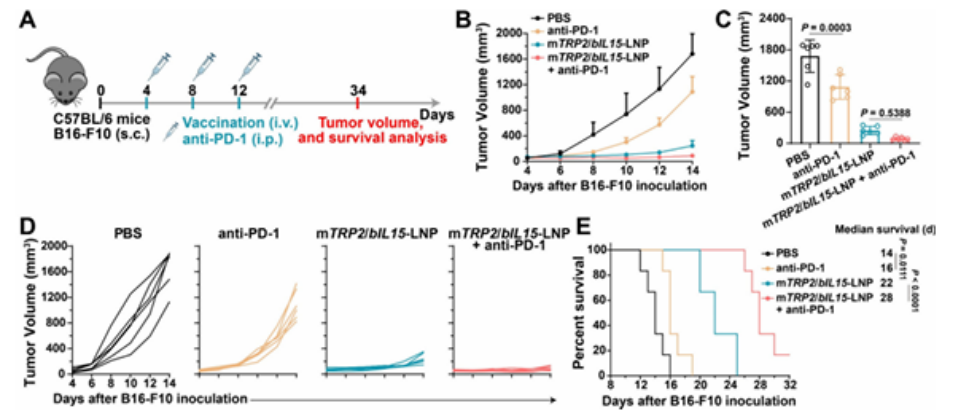
圖例8:mTRP2/bIL15-LNP與抗PD-1聯(lián)合治療在B16F10模型中的效果
7. 疫苗體內(nèi)安全性驗(yàn)證
急性與慢性毒性實(shí)驗(yàn)顯示�����,經(jīng)mTRP2/bIL15-LNP處理后��,小鼠心����、肝��、脾、肺���、腎無(wú)明顯病理?yè)p傷,體重?zé)o顯著下降��,血清中ALT��、AST�、BUN���、CRE����、CK、LDH 等肝、腎、心功能指標(biāo)與對(duì)照組無(wú)顯著差異��,安全性良好。
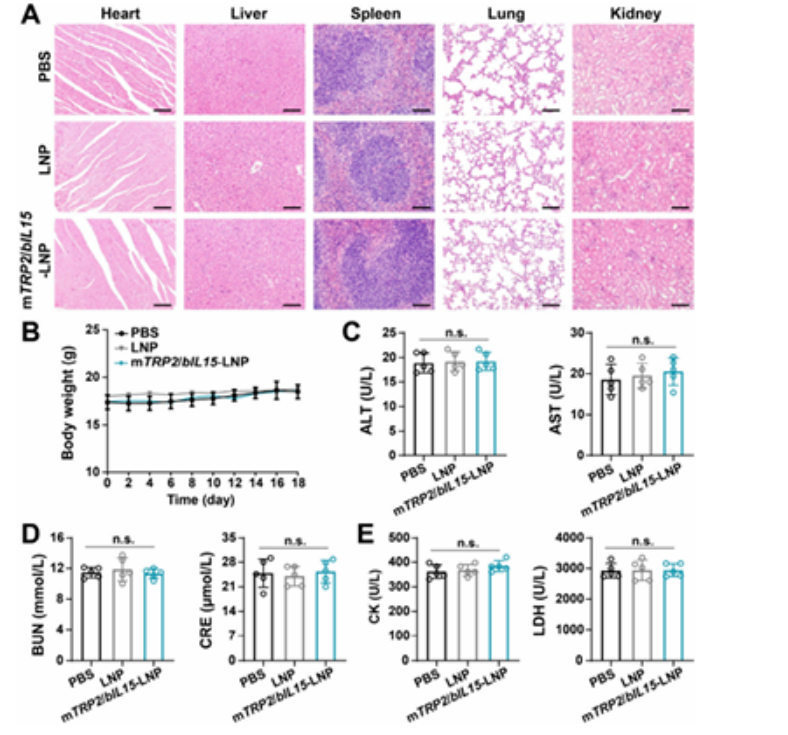
圖例9:mTRP2/bIL15-LNP體內(nèi)安全性評(píng)估
知識(shí)分享:研究亮點(diǎn)
1 提出VISIT策略���,以脾臟靶向的優(yōu)化脂質(zhì)納米粒共遞送腫瘤抗原mRNA與膜結(jié)合型IL-15/IL-15Rα復(fù)合物mRNA,實(shí)現(xiàn)樹(shù)突狀細(xì)胞體內(nèi)重編程�,同步調(diào)控抗原呈遞與T細(xì)胞激活���,解決非特異性免疫激活問(wèn)題����。
2 發(fā)現(xiàn)納米粒表面吸附的talin-1蛋白可通過(guò)與樹(shù)突狀細(xì)胞表面整合素作用增強(qiáng)靶向攝取���,為脾臟定向遞送提供新機(jī)制���。
3 該疫苗在小鼠腫瘤模型中兼具預(yù)防性與治療性效果�,與抗PD-1聯(lián)用顯協(xié)同作用,且安全性良好�,為個(gè)性化癌癥免疫療法提供新范式���。
參考文獻(xiàn):
ACS Nano(IF 16)Pub Date:2025-10-28,DOI:10.1021/acsnano.5c09365.
 歡迎來(lái)到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站!
歡迎來(lái)到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站! 歡迎來(lái)到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站!
歡迎來(lái)到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站!










