2025年6月27日,一篇在期刊《Veterinary Microbiology》上發表題為"A lyophilized anti-rabies mRNA-LNP vaccine induces early and robust immune responses from a single-dose subcutaneous administration"的研究論文,該研究針對狂犬病防控需求,設計并制備了包裹狂犬病糖蛋白mRNA的LNP疫苗,為狂犬病防控提供了安全、高效、便捷的新型疫苗候選方案。

本研究中,核心設備采用艾特森微流控制備儀MPE-L2,成功制備出狂犬病mRNA-LNP疫苗。研究團隊通過該設備的微流控技術精準調控反應條件,結合動態光散射和透射電鏡觀察驗證,所制備的mRNA-LNP疫苗呈單分散球形結構,平均粒徑達132.2nm,分散系數低,zeta電位為-7.45mV,封裝效率超94%,充分彰顯了艾特森微流控制備儀MPE-L2在疫苗制備中兼具精準性與穩定性的優勢,為新型狂犬病mRNA疫苗的理化性能保障提供了關鍵設備支撐。

研究背景
狂犬病是致死率近100%的人畜共患病,全球每年約5.9萬人因感染狂犬病而死,95%由犬類咬傷引發,動物免疫是防控核心。
現有的滅活疫苗需多劑接種,操作繁瑣、成本高,在疫苗覆蓋率低的發展中國家推廣受限;而mRNA疫苗無感染風險、制備快速可規模化,在新冠疫情中展現潛力,可誘導高水平病毒中和抗體,為傳染病防控提供了新方向,但當前狂犬病mRNA疫苗尚未獲批臨床或獸醫應用,且存在免疫途徑效果不佳、單劑難達保護閾值、穩定性不足等問題,亟需開發單劑有效、儲存便利且適用于犬貓的新型狂犬病mRNA疫苗。
1. mRNA-LNP疫苗制備過程
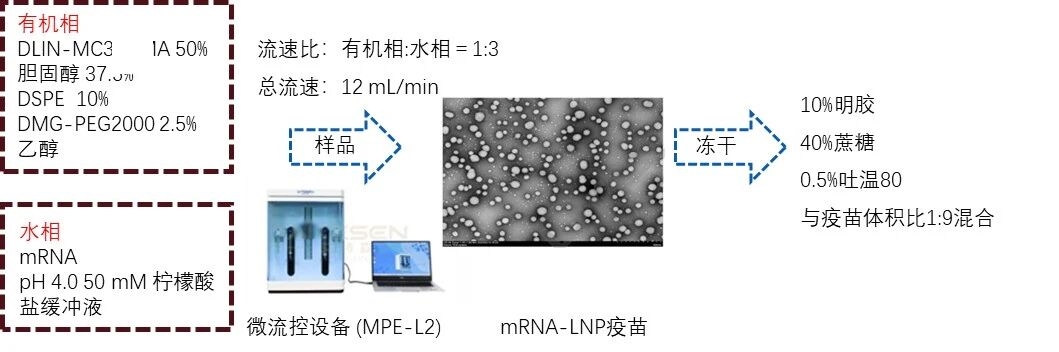
圖例1:mRNA-LNP疫苗制備過程
2. RABV-G mRNA序列結構與蛋白表達驗證
首先,研究團隊明確了RABV-G mRNA的完整結構,包含5’帽結構、非翻譯區、編碼序列及多聚腺苷酸尾;其次,通過直接免疫熒光和Western blot實驗,驗證了mRNA在細胞內的有效表達,通過篩選出高表達的mRNA-C序列,且LNP包裹后的mRNA仍能正常表達目標蛋白,為疫苗構建提供了核心基礎。
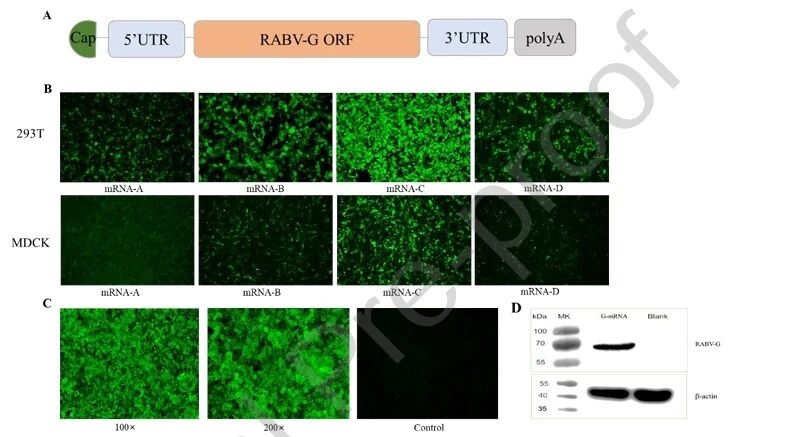
圖例2:RABV-G mRNA序列結構與蛋白表達驗證
3. mRNA-LNP 疫苗的理化特性分析
依托艾特森微流控設備制備的mRNA-LNP疫苗,經檢測具備良好的理化穩定性,這一成果突破了傳統疫苗制備的技術瓶頸,也為解決狂犬病mRNA疫苗穩定性不足、制備規模化難題提供了可行路徑,為后續疫苗的免疫效果優化及獸醫應用轉化奠定了重要基礎。

圖例3:mRNA-LNP疫苗的理化特性分析
4.單劑量mRNA疫苗在小鼠中的體液免疫應答與保護效果
首先,研究團隊通過對比肌內注射與皮下注射途徑,發現皮下注射誘導的病毒中和抗體(VNA)滴度更高,且呈劑量依賴性;其次,免疫后14天抗體滴度即超過0.5IU/mL保護閾值,28天達到峰值并維持穩定;接著,lethal病毒攻擊實驗顯示,免疫小鼠全部存活且體重穩定,證明單劑量疫苗可誘導強效且持久的保護性免疫應答。

圖例4:單劑量mRNA疫苗在小鼠中的體液免疫應答與保護效果
5.疫苗免疫后小鼠腦部組織病理與病毒檢測
團隊通過組織病理學分析發現,未免疫的感染小鼠腦部出現神經元壞死、水腫等嚴重損傷,而免疫小鼠腦部無明顯病理異常;其次,免疫組化結果顯示,感染小鼠腦部可檢測到RABV-N蛋白,免疫組未檢測到,證明疫苗能有效阻止病毒侵入中樞神經系統,避免神經損傷。

圖例5:疫苗免疫后小鼠腦部組織病理與病毒檢測
6.mRNA疫苗在犬貓中的免疫原性與安全性
犬貓皮下免疫后,VNA(Virus-Neutralizing Antibodies,病毒中和抗體)滴度在第4周達到峰值,且顯著高于滅活疫苗,36周后仍維持在保護閾值以上;其次,相同劑量下貓的抗體滴度約為犬的2倍;接著,疫苗在體內主要分布于注射部位和血液,24小時后無殘留;最后,高劑量免疫后動物體溫、食欲等無異常,證明疫苗在犬貓中安全且能誘導長效免疫。
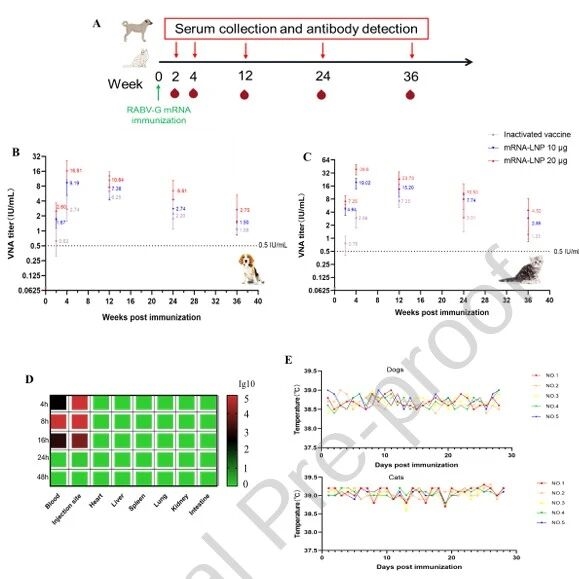
圖例6:mRNA疫苗在犬貓中的免疫原性與安全性
7.mRNA疫苗誘導的體液與細胞免疫應答
流式細胞術檢測顯示,疫苗可顯著增強CD4+和CD8+T細胞應答,而滅活疫苗僅誘導CD4+T 細胞免疫;其次,ELISA結果表明,疫苗誘導的IFN-γ和IL-4水平顯著高于對照組,證明疫苗同時激活Th1和Th2介導的體液免疫與細胞免疫。
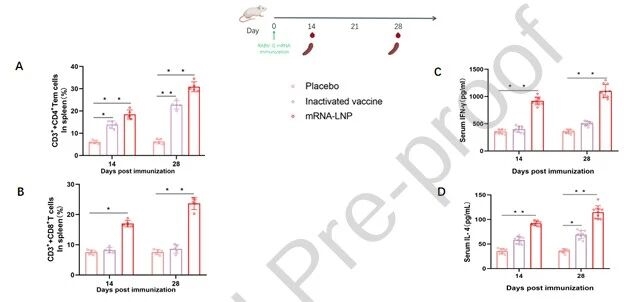
圖例7:mRNA疫苗誘導的體液與細胞免疫應答
8.mRNA-LNP 疫苗的穩定性分析
研究團隊還發現,新鮮疫苗在25℃儲存7天后免疫原性顯著下降,4℃儲存7天免疫原性無明顯變化;其次,凍干疫苗在-20℃儲存4個月后,誘導的VNA滴度與新鮮疫苗相當,6個月后滴度減半,證明凍干工藝可改善疫苗穩定性,滿足-20℃下的中短期儲存需求。
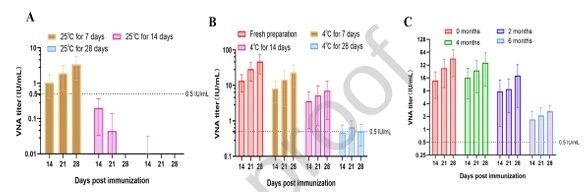
圖例8:mRNA-LNP 疫苗的穩定性分析
知識分享:研究亮點
該研究首次證明凍干mRNA-LNP疫苗單次接種即可實現狂犬病免疫保護,突破了傳統疫苗需多次接種的限制。G蛋白特異性Th2免疫應答和持久的VNA產生是保護關鍵。特別值得注意的是,疫苗在貓科動物中的優異表現為狂犬病主要傳播宿主的防控提供了新方案。
研究團隊指出,該技術路線具有快速適配新毒株的潛力,且凍干工藝解決了mRNA疫苗的儲存難題。
參考文獻:
Veterinary Microbiology Pub Date: 2025-06-27, DOI: 10.1016/j.vetmic.2025.110612.
 歡迎來到蘇州艾特森制藥設備有限公司網站!
歡迎來到蘇州艾特森制藥設備有限公司網站! 歡迎來到蘇州艾特森制藥設備有限公司網站!
歡迎來到蘇州艾特森制藥設備有限公司網站!









