2025年3月28日 ,阿法納生物與中國科學技術大學王育才教授團隊合作,《Nature Biomedical Engineering》上發表題為" Generation of tolerogenic antigen-presenting cells in vivo via the delivery of mRNA encoding PDL1 within lipid nanoparticles "的研究論文。

研究先是以Moderna COVID-19 mRNA疫苗的LNP配方為參考,根據田口正交陣列設計創建9種LNP配方,通過艾特森MPE-L2型微流控設備儀完成樣品制備,為后續小鼠皮下給藥、不同配方免疫原性評估及低免疫原性配方篩選提供了精準的實驗制備支撐,是實現低免疫原性LNPs配方優化與驗證的關鍵實驗環節。

研究背景
文獻中創新性地構建了低免疫原性脂質納米顆粒(LNPs)遞送PD-L1 mRNA,在體內直接編程生成耐受性抗原呈遞細胞(tol-APCs),在類風濕性關節炎與潰瘍性結腸炎等自身免疫病模型中展現出療效,實現無需體外細胞操作、直接在體內構建功能性tol-APCs的治療策略。該策略不僅能選擇性抑制致病性T細胞活化,還能擴大調節性T細胞(Tregs)群體,真正實現“精準抑制病灶、重建免疫耐受”的自免治療新機制,具有很強的疾病特異性和長期療效潛力。
1. 核心概念與機制框架
針對傳統tol-APCs 體外制備的復雜性,研究團隊提出 “低免疫原性mRNA遞送+體內原位生成tol-APCs”的核心策略,同時明確其治療機制:tol-APCs通過PDL1/PD1通路,選擇性靶向高表達PD1的激活T細胞(誘導其凋亡、抑制其增殖),并促進調節性T細胞(Treg)擴增,且不影響低表達PD1的初始T細胞,為后續實驗設計奠定明確方向。

圖例1:核心概念與機制框架
2. 實驗過程
? 通過 Design of Experiments 選擇低免疫原性的LNPs

圖例2:配方篩選
通過艾特森MPE-L2微流控設備制備樣品后,對小鼠皮下給藥,評估不同配方的免疫原性,結果中發現脂質組成(摩爾比)和N/P比均對LNPs的轉染效率和免疫原性有顯著影響,在9組中選取低免疫原性的配方,以避免在AIDs治療中引發意外的免疫反應。
? 低免疫原性LNPs/mPDL1制備工藝條件

圖例3:LNPs/mPDL1制備過程
? 制備包載PDL1 mRNA的LNPs

3. 低免疫原性LNPs的篩選優化
基于圖例1對載體的低免疫原性需求,圖例4通過實驗設計(DOE)完成載體篩選,以EGFP mRNA為報告基因,檢測淋巴結樹突狀細胞(DCs)的共刺激分子(CD80、CD86、CD40)表達,最終篩選出A7配方(SM-102:DSPC:DMG-PEG2000: 膽固醇=25:5:0.5:69.5,N/P=4),其共刺激分子表達最低,為mRNA遞送提供理想載體。
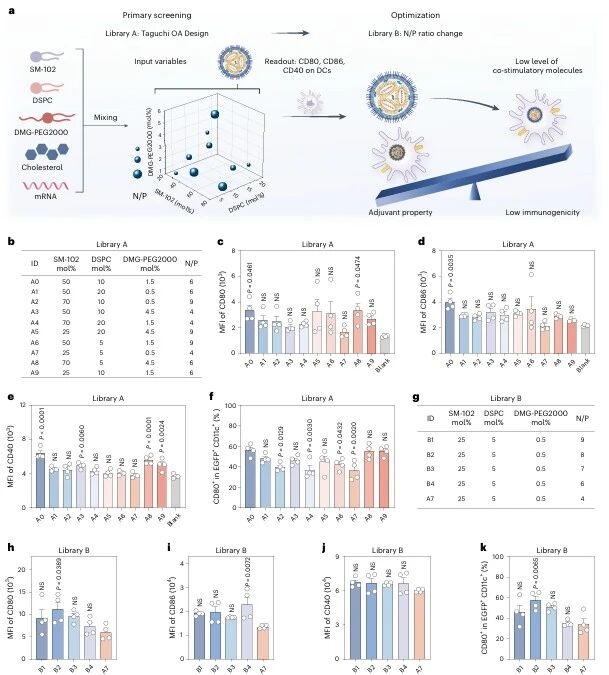
圖例4:低免疫原性LNPs的篩選優化
4.LNPs/mPDL1體內外生成tol-APCs
載體優化后,研究團隊驗證核心功能:體外實驗中,DC2.4和RAW264.7細胞經LNPs/mPDL1處理后,表面 PDL1表達顯著升高;體內實驗中,小鼠皮下注射LNPs/mPDL1 后,淋巴結、脾臟、外周血中的CD11c +和 CD11b+ APC 高表達PD1,骨髓中無tol-APCs 生成,且 tol-APCs可持續存在至少4天,該方法僅靶向APC,對非APC免疫細胞影響極小。
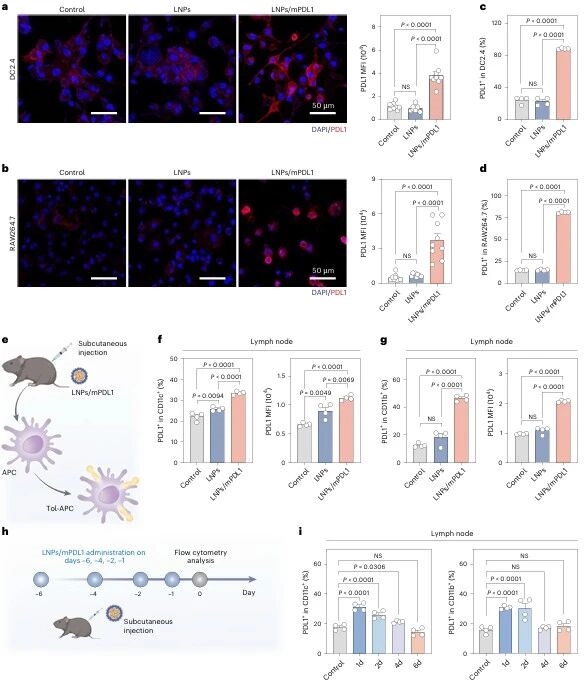
圖例5:LNPs/mPDL1體內外生成tol-APCs
5.tol-APCs對激活T細胞的體外調控
為驗證tol-APCs的調控功能,研究團隊開展體外實驗:激活的T細胞高表達PD1,與LNPs/mPDL1誘導的tol-APCs共培養后,CD4+和 CD8+T細胞增殖顯著受抑,且tol-APCs可誘導激活T細胞凋亡,不影響初始T細胞,激活T細胞caspase-3/7活性增強,佐證凋亡通路參與調控。

圖例6:tol-APCs對激活T細胞的體外調控
6.tol-APCs對激活T細胞的體內選擇性清除
體外機制明確后,研究團隊通過過繼轉移實驗驗證體內效果:用CFSE標記區分激活T 細胞(高CFSE)和初始T細胞(低CFSE),輸注給預先注射LNPs/mPDL1的裸鼠,結果顯示LNPs/mPDL1處理組中,激活T細胞占比、激活/初始T細胞比值顯著降低,CD4+和CD8+激活T細胞被選擇性清除,初始T細胞比例升高,驗證了治療的安全性和特異性。

圖例7:tol-APCs對激活T細胞的體內選擇性清除
7.RA模型中tol-APCs的治療效果
機制驗證完成后,研究團隊將策略應用于類風濕關節炎(RA)模型:DBA/1小鼠經Ⅱ型膠原蛋白免疫誘導RA,給予LNPs/mPDL1、空LNPs、依那西普(臨床RA治療藥物)或PBS處理,結果顯示LNPs/mPDL1組關節炎指數、爪墊腫脹程度顯著降低,關節軟骨損傷減輕,炎癥因子(IFN-γ、TNF-α)水平降低,淋巴結中促炎CD4+T細胞減少、Treg細胞增多,療效與依那西普相當。
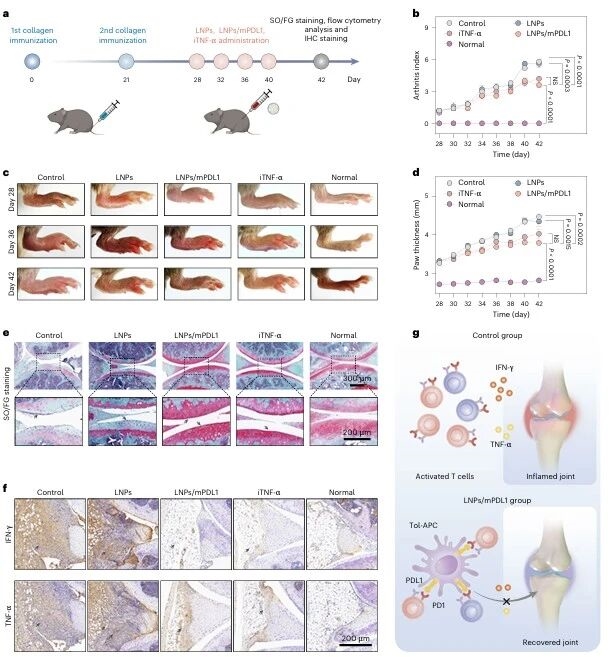
圖例8:RA模型中tol-APCs的治療效果
8.UC模型中tol-APCs的治療效果
為證明策略普適性,研究團隊將其拓展至潰瘍性結腸炎(UC)模型:C57BL/6小鼠飲用3%DSS水溶液誘導UC,給予LNPs/mPDL1、空LNPs、環孢素(臨床UC治療藥物)或PBS處理,結果顯示 LNPs/mPDL1組疾病活動指數(DAI)降低,體重下降和結腸縮短現象改善,腸道黏膜損傷減輕,腸系膜淋巴結中Th17細胞減少、Treg細胞增多,療效與環孢素相當。
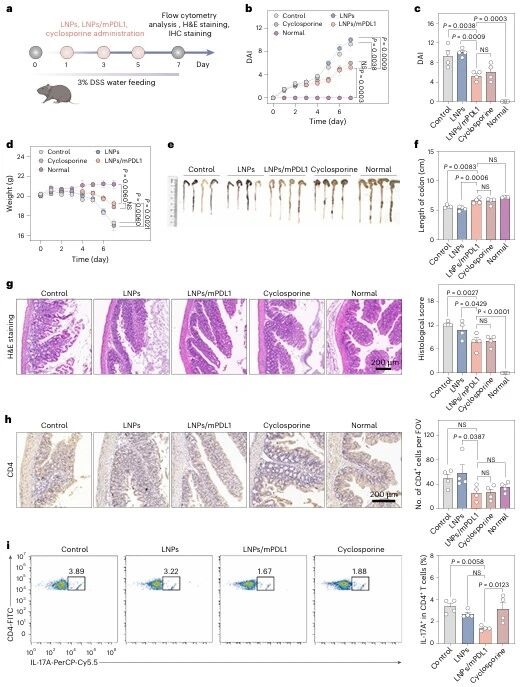
圖例9:UC模型中tol-APCs的治療效果
知識分享:研究亮點
1 低免疫原性脂質納米粒(LNPs)設計:通過優化脂質成分及氮磷比(N/P),開發出低免疫原性的LNPs/mPDL1遞送系統,顯著減少APC表面共刺激分子(如CD80、CD86、CD40)的表達,避免傳統LNPs的佐劑效應,從而抑制非特異性免疫激活;
2 體內原位生成致耐受性APCs:利用mRNA技術,通過皮下注射LNPs/mPDL1,直接在體內誘導APCs高表達PDL1,生成tol-APCs,選擇性靶向活化的PD1和 T細胞并誘導其凋亡,同時保留初始T細胞;
3 廣譜治療潛力與臨床轉化優勢:在類風濕性關節炎(RA)和潰瘍性結腸炎(UC)小鼠模型中,LNPs/mPDL1顯著緩解炎癥、減少致病性Th1/Th17細胞、增加調節性T細胞(Treg),療效媲美臨床藥物(如依那西普、環孢素),為自身免疫病及器官移植耐受提供了新策略。
參考文獻:
Nature Biomedical Engineering ( IF 26.8 ) Pub Date:2025-03-28,DOI: 10.1038/s41551-025-01373-0.
 歡迎來到蘇州艾特森制藥設備有限公司網站!
歡迎來到蘇州艾特森制藥設備有限公司網站! 歡迎來到蘇州艾特森制藥設備有限公司網站!
歡迎來到蘇州艾特森制藥設備有限公司網站!











