2024年8月10日 上海交通大學章雪晴團隊與新澤西理工學院許曉陽團隊在期刊《Nature Communications》上發表題為" Optimized inhaled LNP formulation for enhanced treatment of idiopathic pulmonary fibrosis via mRNA-mediated antibody therapy "的研究論文。

研究團隊初步設計了7種不同脂質摩爾比的LNP制劑,經艾特森MPE-L2型微流控制備儀制備樣品后,為后續制劑篩選與理化性質評估提供了試驗基礎。

研究背景
特發性肺纖維化(IPF)是高死亡率的間質性肺病,現有藥物僅能延緩病程,無法逆轉瘢痕;基于 mRNA 的蛋白替代療法雖具潛力,但mRNA穩定性差、轉染效率低,需依賴有效遞送系統。
脂質納米顆粒(LNPs)在相關藥物和疫苗中展現價值,卻存在肺部靶向性不足的問題,而吸入給藥雖為呼吸系統疾病的理想途徑,卻面臨霧化剪切力損傷等多重挑戰,目前尚無吸入性LNP-mRNA候選藥物完成臨床試驗,因此亟需開發具備轉化潛力的吸入性LNP遞送系統及便捷篩選方法,因此,研究團隊開發了新的LOOP平臺遞送mRNA。
1. 制備過程

圖例1:LNP制備過程
2. 篩選過程
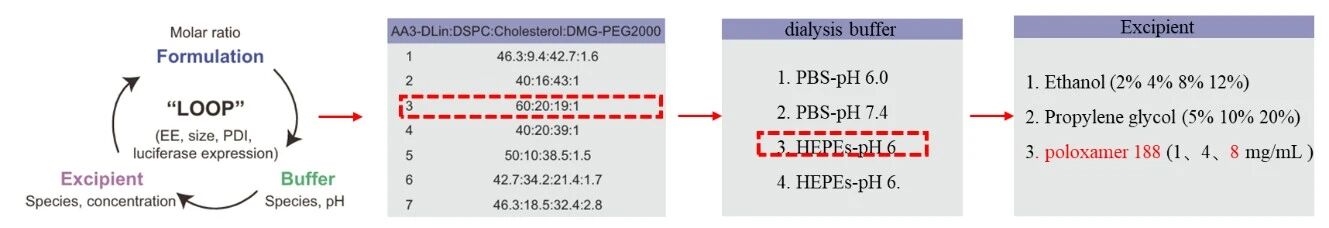
圖例2:LNP篩選過程
3. scFv@iLNP-HP08LOOP治療IPF的吸入遞送機制
研究團隊初步明確了”scFv@iLNP-HP08LOOP”的核心作用路徑,該遞送系統經吸入后可抵抗霧化剪切力,進入肺間質并被多種細胞內化,隨后通過溶酶體逃逸釋放IL-11 scFv mRNA,在核糖體的作用下翻譯為IL-11 scFv,最終通過自分泌或旁分泌方式結合IL-11,阻斷下游纖維化信號通路。

圖例3:scFv@iLNP-HP08LOOP治療IPF的吸入遞送機制圖
4. 霧化mRNA遞送用iLNP的“LOOP”篩選流程與結果
研究團隊初步設計的7種不同脂質摩爾比的LNP制劑,經過艾特森MPE-L2微流控制備儀制備樣品后,通過評估霧化前后的包封效率、粒徑及PDI的變化,篩選出LNP-3作為候選制劑;隨后探究不同透析緩沖液的影響,發現pH 6.0的HEPEs可使LNP霧化后理化性質變化最小,確定為較好透析條件。這一篩選流程明確了iLNP 優化的核心指標與關鍵緩沖液參數,為后續引入輔料改善霧化穩定性提供了基礎。
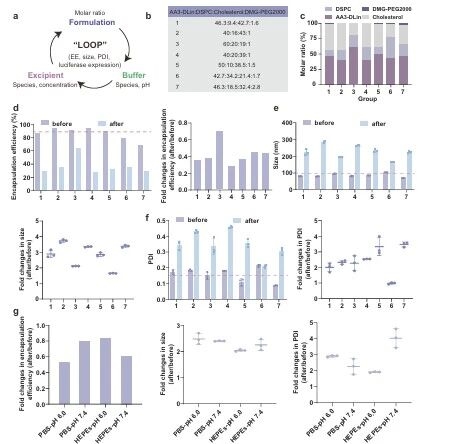
圖例4:霧化mRNA遞送用iLNP的“LOOP”篩選流程與結果
5.輔料對霧化iLNP性能的改善作用
進一步地,研究團隊在霧化緩沖液中引入乙醇、丙二醇、泊洛沙姆188三種輔料,發現其可通過降低表面張力、增加溶液粘度提升LNP霧化穩定性,且輔料濃度與肺部熒光素酶表達呈正相關;隨后對比安全性與表達效率,確定8mg/mL泊洛沙姆188為最終霧化緩沖液,該緩沖液還可增強市售ALC0315 LNPs的穩定性。

圖例5:輔料對霧化iLNP性能的改善作用
6. iLNP-HP08LOOP的理化性質與生物特性表征
研究團隊為明確脂質組成與活性的關系,通過制備mEGFP@iLNP-HP08 LOOP,經檢測發現其在生理條件下穩定性良好,能有效保護mRNA不被降解,且轉染效率呈劑量依賴性;隨后通過抑制實驗證實其主要經網格蛋白介導的內吞作用進入細胞,同時具備快速溶酶體逃逸能力,且無明顯細胞毒性,霧化前后結構與包封效率保持穩定。這些表征結果驗證了 iLNP-HP08LOOP 平臺具有優秀的遞送潛力。
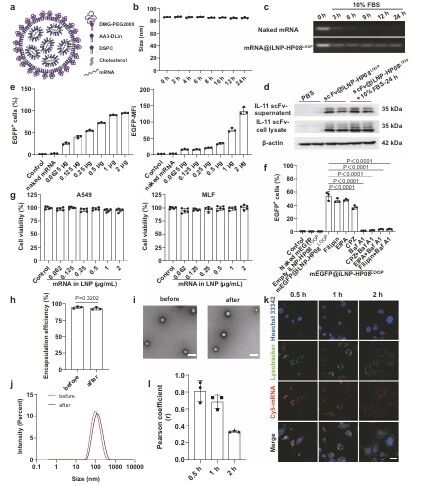
圖例6:iLNP-HP08LOOP的理化性質與生物特性表征
7. scFv@iLNP-HP08LOOP對MLFs分化、遷移及侵襲的抑制作用
接著,研究團隊將編碼IL-11 scFv 片段的mRNA封裝于iLNP中,發現其轉染MLFs后,IL-11 scFv呈劑量依賴性持續表達并有效結合IL-11;隨后通過免疫熒光與Transwell實驗證實,該制劑能顯著抑制TGF-β1/IL-11誘導的成纖維細胞活化、ECM沉積及遷移侵襲能力,且可下調下游p-ERK 信號通路。

圖例7:ASFV-ΔE120R體內安全性及無病毒殘留驗證
8. scFv@iLNP-HP08LOOP抑制小鼠博來霉素誘導的肺纖維化
通過建立小鼠肺纖維化模型,設置多種給藥對照組,經形態觀察、器官系數計算、免疫熒光染色等檢測結果,研究團隊發現,吸入scFv@iLNP-HP08LOOP能顯著減輕肺組織損傷與僵硬程度,降低羥脯氨酸含量及纖維化標志物表達;隨后對比不同給藥方式,證實其療效優于靜脈注射和直接吸入IL-11 scFv,且在支氣管肺泡灌洗液中能維持更長時間的高表達。

圖例8:scFv@iLNP-HP08LOOP抑制小鼠博來霉素誘導的肺纖維化
9. 肺組織組織學評估與IL-11下游信號通路分析
研究團隊對小鼠肺組織進行多組學染色,發現scFv@iLNP-HP08LOOP可顯著改善肺泡隔增厚,減少膠原纖維產生,對肺組織結構修復效果突出;隨后通過Western blot檢測證實,其抗纖維化作用主要通過抑制IL-11下游p-ERK信號通路實現,而STAT3通路不受影響。這一機制解析明確了制劑的作用靶點,為臨床應用提供了理論支撐。
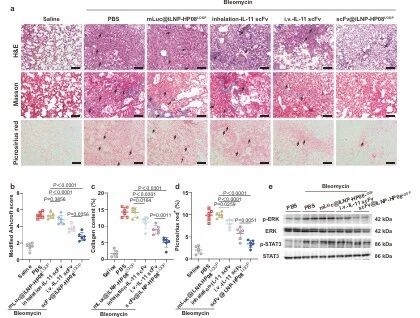
圖例9:肺組織組織學評估與IL-11下游信號通路分析
10. scFv@iLNP-HP08LOOP 恢復纖維化小鼠的肺功能
研究團隊采用強迫振蕩技術檢測肺功能參數,發現博來霉素誘導的纖維化小鼠呼吸阻力、彈性顯著升高,吸氣容量、肺活量等指標顯著降低;隨后證實吸入scFv@iLNP-HP08LOOP能有效逆轉這些異常指標,使肺部內在彈性恢復接近健康水平。肺功能的顯著改善凸顯了該制劑的臨床潛力。

圖例10:吸入scFv@iLNP-HP08LOOP恢復纖維化小鼠的肺功能
知識分享:研究亮點
1 創新提出“LOOP”四步篩選平臺,無需大量篩選即可獲得抗剪切力強、表達效率高的吸入性脂質納米顆粒(iLNP),還可增強市售ALC0315 LNPs的穩定性。
2 構建iLNP-HP08LOOP制劑,通過高輔助脂質比例、酸性透析緩沖液及含泊洛沙姆188的霧化緩沖液,實現mRNA的高效遞送與穩定表達。
3 開發mRNA介導的IL-11 scFv吸入療法,相較于傳統抗體給藥方式,更高效抑制肺纖維化,且顯著改善模型小鼠肺功能,為呼吸系統疾病治療提供新路徑。
參考文獻:
Nature Communications (IF 15.7) Pub Date: 2024-08-10 , DOI: 10.1038/s41467-024-51056-8.
 歡迎來到蘇州艾特森制藥設備有限公司網站!
歡迎來到蘇州艾特森制藥設備有限公司網站! 歡迎來到蘇州艾特森制藥設備有限公司網站!
歡迎來到蘇州艾特森制藥設備有限公司網站!











